皆様お疲れ様です🌱
raikaです。
今回は久しぶりのお勉強系の記事にしようと思います✍️
今回のお題は『pH』です。
マリンアクアリウムでは塩分や水温に並ぶほど必須の項目で、pHを知らない方は居られないと思います。当然ですが推奨される適正値が存在し、これを大きく逸脱すると生体に悪影響を及ぼします。ただし、水槽内では様々な生命活動や化学反応の結果、特に気にしなくてもバランスが自然と取られている事がほとんどです。この為、栄養塩や必須元素ほど細やかに気を配る事は少ないのかも知れません。酸性やアルカリ性を示す数値である事は広く知られた事ですが、さらに深掘りする機会はなかなか無いように思います。
今回はそんな『pH』について学んでみようと思います。基本的な内容を私なりにできるだけ分かりやすく解説し、個人的に気になる内容やどう管理すべきかなどをまとめてみようと思います✍️
そもそもpHって何なのか?
小難しい話になりますが、まずはpHとは何なのかについてまとめておきます。
pHとは『溶液の水素イオン濃度を指数で表したもの』で、『ピーエイチ』や『ペーハー』と呼ばれます。後者はドイツ語読みであり、医者である私にとっては『ペーハー』の呼び名で慣れ親しんだ言葉です。語源には諸説あるようなので、ここでは割愛します。
前述のごとく、pHは単に水素イオンの濃度を表すものではなく、常用対数という高校生で学んだ数式により手が加えられて指数化されています。詳しくは水素イオン濃度(以降[H+]と表記)のモル濃度をmol/L単位で表した数値の逆数の常用対数にほぼ近似します。
pH≒-log10[H+]
この式を見ると途端にアレルギー反応が出て、「もういいです…💦」となるかも知れませんが、大事な事は数式を覚えることではないので、ここは「そうなのね😌」と流し読みで構いません🙆♂️
ポイントとしてはlog10、つまり常用対数を使用して導き出されている点です。
常用対数とは、ある正の数 x に対して、x = 10a という数式があった場合、 a を、10 を底とする x の常用対数 と呼び、記号を用いて log10 x で表すことになっています。つまり、以下のような関係性が成立します。
x = 10a ⇔ a = log10x
まだ全然分かりにくいと思いますが、例えばaが1であればXは10、aが2であればxは100、aが3であればxは1000というように、aの変化に対してxはかなり大きな変化が出ます。これをpHに言い換えると、pHが1変化すれば、水素イオン濃度は10倍の変化が生じているということになります。通常の水槽内でpHが1も変化することは中々ありませんが、pH0.3の変化で水素イオンは約2倍、0.6の変化で約4倍変わります。

pHで表すと微細な変化でも、水素イオンとしてはかなりの変化が起こっている事は認識しておくと良いと思います。
pHはアクアリウムで測定される以外にも、河川の水や食品、医療分野では血液であったり、色々な溶液に用いられ、その溶液の質を測る一手段として用いられています。
アクアリウムにおける『pH』
pHが水素イオン濃度を表す指標である事が掴めたところで、次はこの数値をアクアリウムではどのように利用するか考えていきます。
pHは我々医療現場でも非常に大切な血液検査項目の一つです。その意義としては、簡潔に表すと『肺や腎臓などの重要臓器の機能不全を察知する指標』、言い換えると『各々の重要臓器が正常に機能しているかの指標』とも言えます。
アクアリウムでも同じような感覚なのかなと思います。つまり、pHが表す水素イオン濃度自体が直接生体の健康に影響するからpHを測定しているわけではなく、『pHが変動するような外的要因の有無を評価するために測定する』、『水槽内で起こる様々な反応のバランスが安定しているか確認するために測定する』と考えた方が良いと思います。そして加えて、pHが大きく異常値であれば、その状態の飼育水が魚やサンゴの健康や成長に悪影響を与えることも重要です。
なので、pHに変動があれば、次にそれを起こしている原因を考えることが大事なのです。原因を同定せずにpHのみを補正することも可能ではありますが、それは臭い物に蓋をしているだけであって、状況によっては大きな損失となる場合もあります。
pHには他のパラメーターと同様に推奨値があります。書籍やネットの情報により若干の幅がありますが、ざっくりと7.8〜8.4程度の間に収まっている場合がほとんどかと思います。そしてこの数値は水槽内の生命活動により日内変動します。一般的に光合成活動が増える日中は高く、夜間は低いというものです。我が家の水槽の場合は以下のような感じになります。
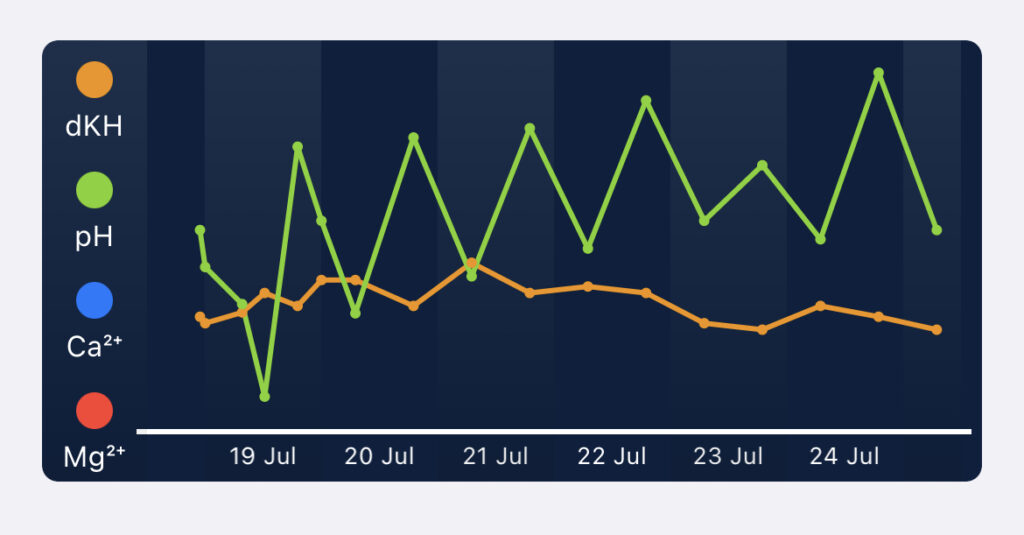
図中の緑がpHの振れ幅で昼間と夜がジグザグになっているのが見てとれると思います。
下は約7.9、上は約8.1程度で推移しています。
pHは各個人の水槽内の環境で数値がある程度異なります。このため、理想値を追い求めるよりは、一般的な推奨値の範疇にあり、ご自身の水槽の日中の動きをある程度把握した上で、これを逸脱するような事が起きないか否かに注意を払うと良いと思います。
では次に、普段のサイクルから逸脱する場合、どういった事が原因になりうるかをみていきます。マリンアクアリウムにおけるpHの異常は、何らかの要因で異常に下降してしまうパターンが主体です。逆に、pHが高いから何とかして下げるという局面はあまりないかなと思います。この下降要因には色々ありますので、ここでは代表的なものを紹介します。
二酸化炭素はpHを下げる要因の代表格です。pHが下がる、つまりH+が増える理屈は以下の化学式の通りです。
- CO2 + H2O ⇄ H2CO3
- H2CO3 ⇄ H+ + HCO3-
- HCO3- ⇄ H+ + CO32-
化学式は、式を構成する一方の物質の量が増えると、平衡を保つ方向に反応が進みます。このため二酸化炭素が増えると、①式は右に進み炭酸(H2CO3)となります。これによって増加した炭酸は②式を右に進めます。これによって増えた水素イオンは一部消費されて③式を少し左に進めます。結果的に、炭酸イオンが低下し、水素イオンが増加して、pHは低下します。
水槽内で二酸化炭素が増える要因にはいくつか考えられます。暖房などの影響で室内の二酸化炭素が高い、生体が多く、それらの呼吸により二酸化炭素が上昇するなどです。
この場合、ここで問題となるのはpHが下がった事よりも、炭酸イオンが低下した事です。これは環境問題の一つ、『海洋酸性化』と全く同じ状況で、炭酸カルシウムの材料が減るなどして、サンゴや貝など、炭酸カルシウムの骨格を形成する生体に大きな悪影響を及ぼすのです。
主に好気性菌が活動(硝化)を活発に行うことで、その代謝物として栄養塩と共に水素イオンが発生します。原料となる残り餌や排泄物などが多かったり、好気性バクテリアのバランスが過多であったりするとpHに影響する可能性があります。
上記のような要因で下降するpHですが、実際の水槽内ではある程度の範囲で自然と維持され、極端な下降はなかなか起こりません。こういった極端な動きを抑制してくれる作用を緩衝作用と呼びます。『pH』の変動に対する緩衝作用は『KH』によりもたらされます。
『KH』については以前の記事で詳細に触れましたが、炭酸イオンと重炭酸イオンの総量とも捉えることができる数値です。
ここでもう一度前述の化学式に登場してもらいます。
- CO2 + H2O ⇄ H2CO3
- H2CO3 ⇄ H+ + HCO3-
- HCO3- ⇄ H+ + CO32-
この化学式がもし二酸化炭素の存在で、前述のような動きで均衡が崩れそうな際に、炭酸イオン(CO32-)や重炭酸イオン( HCO3-)があれば、その均衡を保つ方向に働いてくれるのです。
『pH』の理想値について考える🤔
pHは前述した通り、基本は良い塩梅でバランスが保たれており、無理にそれを修正する必要はないかなと私は思います。
それよりは、日々の推移を把握しておき、そこからの逸脱を水槽全体の異変として察知する為に利用すると良いかと思います。もちろん、日々の数値がかなり低め(7に近い)であれば、その時点で原因検索は必要かと思います⚠️
ただし、さらに良い環境を目指す方にとっては、pHのより理想的な数値というものも気になるところかと思います。
私が調べた限りでは、推奨されている範囲内で高めとなる8.2あたりが理想かと考えました。その理由としては、高めのpHは炭酸カルシウムの形成が促進されると考えられており、これはすなわちサンゴの骨格形成を促進する事に繋がるためです。
サンゴの骨格である炭酸カルシウムは、およそpH8.5以上のアルカリ環境下で形成が促進されます。これは炭酸物質であり炭酸カルシウムの原料となる炭酸イオンの割合がpHg8.5以上の環境で増えるためです。このpH環境を、サンゴは自身の体内にある『石灰化母液』と呼ばれる体液内で実現させており、この体液内で骨格の材料となる炭酸カルシウムを作り出すと考えられています。この体液内に水中にあるカルシウムと炭酸イオンを引き込む為には濃度勾配に逆らう為のエネルギーを使います。飼育水環境が石灰化母液に近い性質であれば、そのエネルギーが節約され、結果的に骨格形成しやすくなるという理論です。
ただし、飼育水自体のpHが仮に8.5以上となってしまうと、サンゴの体内に入る前に炭酸カルシウムの形成/沈殿が促進されてしまいます。こうなると、カルシウムやKHを添加しても数値が上がらないという状況に陥るので、上げすぎは良くないです。また、そもそもpH8.5程度の数値というものを実現させるのは難しいようにも思います。
従って、pHの理想値は現実的なラインとして8.2と考えました。
ただし、pHの上昇は緩衝作用を持つKHにも影響を与えます。そしてKHが変動すれば、カルシウムも変動します。そういった変化が飼育される方の許容範囲か否かは注意して調整が必要かと思います。
『pH』の調整
『pH』調整の意義としては、異常に低いpHを正常バランスに戻す場合と、安定しているpHをさらに理想値に近づける場合の2種類があるのかと思います。
この場合は、何かしら水槽内で問題が起きている事がほとんどだと思います。これに関しては積極的に補正が必要です。すでに紹介していますが、改めて代表的な原因とその対処法を記載します。
何らかの原因で大気中の二酸化炭素分圧が上昇すると、水槽へ溶け込む量も増えてpHは低下します。よくある原因は換気不足と石油ファンヒーターの使用です。これらの要因で大気中の二酸化炭素濃度は容易に数倍になります。逆に言えば、換気をしっかり行い、暖房をエアコンにするなどすれば改善も容易です。
水槽内で呼吸を行う生体が過剰であれば、それも二酸化炭素の上昇につながります。また、必然的に餌は多くなり排泄物も増え、これもpH上昇の原因となります。過剰に生体を入れているようであれば、少し減らす事を検討してもいいかも知れません。
前述の項目に関連しますが、餌や排泄物などは好気性菌により硝化されます。この際に水素イオンが発生し、pHが上昇低下します。この場合は栄養塩の蓄積が主体となってくるので、濾過機能を強化したり、換水量や頻度を上げたりするなどが効果的かと思います。
この場合に注意すべきは、単にpHのみを上げることに収支しないことです。炭酸ナトリウムや重炭酸ナトリウムなどのpH上昇剤は数多く市販されていますが、これらを安易に使用すれば、KHやカルシウムなどその他の項目にも少なからず影響が出ます。そういった観点から、私自身が人に提案できる方法は『リフジウム』です。
リフジウムとは、メイン水槽と連結隔離した環境内で海藻を飼育する手法です。
海藻は光合成を行う際に二酸化炭素を消費します。その結果、pHを上昇させる効果があります。その効果はpHの日内変動を見てもらえば明らかかと思います。
またその他にも、リン酸塩や硝酸塩などの栄養塩を吸収する作用があり、水質濾過作用が期待できます。加えて、魚などの大型生体から隔離された領域で海藻を育てることにより動物性プランクトンが繁殖します。増えたプランクトンはメイン水槽に供給され、水槽全体に生物多様性を付与します。これにより、有害な生体の過剰増殖を抑制したり、魚やサンゴの栄養面の底上げにもつながります。
非常に恩恵が多く、自然に近い形で水質を向上させることができるので、私個人としてはお薦めできるシステムです。水槽管理が難しい場合などは、以下のような海藻リアクターを用いるのも良いかと思います👇
こちらは私自身は実践したことはありませんが、pHを上昇させる効果があります。
カルクワッサーは、水酸化カルシウムの飽和溶液を添加する手法で、主にカルシウムの補充とpHの上昇効果が得られます。KHに関しては、使用に際し多少の炭酸カルシウムの沈澱が生じるため、結果的に下がる傾向にあるようです。投与量が多く、微量持続投与が必要であったり、pHの急変のリスクがあるなど、使いにくい側面もあるようです。安易に人には勧められませんが、実際にうまく使っている方もおられますのでここで紹介のみしておきます。
今回は以上になります。pHはこだわり出すとドツボにハマる可能性もあるので、基本はいつものバランスをモニタリングする程度が良いのかと思います。今回の記事で何か得られるものがあれば幸いです🌱
ではまた👋




こんにちは
現在pH低下で悩んでおりraikaさんの記事がとても勉強になりました。ありがとうございます!
もしよろしければ下記1点質問させていただけますと幸いです。
“『pH』の調整”で、餌や排泄物は好気性菌によって消化されその際水素イオンが発生しpHが上昇する、と書かれていますが、
この場合水素イオンが増えてpHが下がるように思うのですが、もしよろしければpH上昇の仕組をご教示いただけますと嬉しく思います。
酸化の亢進
前述の項目に関連しますが、餌や排泄物などは好気性菌により硝化されます。この際に水素イオンが発生し、pHが上昇します。
ゆきまるさん
コメントありがとうございます。
ご指摘の項目ですが、これはゆきまるさんの仰る通り、参加なのでpHは下がります💦 僕の記載ミスです…。変に悩ませてすみません。修正させて頂きます🙇